어스바이오는 Axis Pharm 전문 취급점입니다.
어스바이오 전문 취급점 Axis Pharm의 새로운 소식을 전해드립니다.
Next-Generation of Novel Antibody-Drug Conjugates: Click Chemistry ADCs
현재 임상 환경에서 사용되는 ADC(항체-약물 접합체)는 대부분 효과적인 내부화 및 세포 내 리소좀으로의 이동을 통해 링커의 생분해를 달성하고, 이어서 약물을 방출하는 방식에 의존합니다. 또한, 방출된 약물은 치료 효과를 발휘하기 위해 리소좀에서 탈출해야 합니다. 그러나 모든 종양 항원이 ADC의 효과적인 처리를 보장하지는 않으며, 특히 고형 종양에서는 더욱 그렇고, 현재의 내부화된 ADC는 획득된 종양 저항성 메커니즘에도 민감합니다.
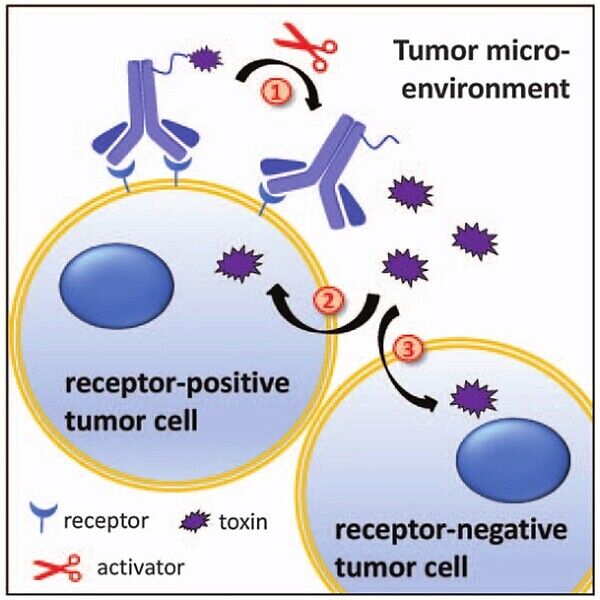
종양 미세환경(TME)에서의 세포외 ADC 분해는 기존의 ADC에 대한 유효한 대안이 될 수 있습니다. 이 경우, 약물이 방출되면 수동적으로 종양 덩어리에 확산되어 이웃한 항원 음성 종양 세포를 침투하고 죽여서 "바이 스탠더 효과"를 극대화할 수 있습니다. 고형 종양에서 TME를 구체적으로 표적화하는 것은 세포막에 풍부하게 존재하는 약한 또는 비내부화 항원(CAIX, VEGFR, 칼레티큘린)이나 세포 외 기질 구성 요소(피브로넥틴 및 테나신-C의 스플라이스 변형체, 피브리노겐, 콜라겐 IV, αvβ3 인테그린) 또는 TME에서 종양 세포에 의해 분비된 단백질(VEGF) 등을 이용하여 달성할 수 있습니다. 약물이 TME에서 선택적으로 방출될 수 있다면, 이 모든 것들은 ADC 치료의 훌륭한 표적이 될 수 있습니다.
비내부화 종양 표적을 표적화한 생분해성 ADC의 중요한 치료 효과는 이황화물 또는 펩타이드 기반 링커를 기반으로 한 연구에서 발견되었습니다. 이황화 결합을 포함하는 커넥터의 세포외 분해는 죽은 세포에서 방출되는 환원제(글루타티온 등)로 인해 발생하며, 이는 더 많은 세포 사멸을 초래하여 더 많은 환원제를 방출하는 것으로 생각됩니다. 또한, 종양 세포 외부에서 종양 혈관 신생, 침습 및 전이에 관여하는 단백질 분해 효소(조직 단백질 분해 효소, 매트릭스 금속 단백질 분해 효소 및 우로키나제형 플라스미노겐 활성화제 등)의 수준이 상승하며, TME에서 세포외 비내부화 항원 프로테아제 민감 단백질을 표적화한 ADC는 여러 마우스 이종이식 모델에서 효과적임이 입증되었습니다. 그러나 세포 내 생분해와 비교하여 세포외 생분해는 보편적이지 않고 효율성이 떨어집니다. 따라서 최근 연구자들은 ADC 커넥터를 위한 화학적 유발 방법을 탐구하고 있습니다.
Axis Pharm 제품의 견적 또는 문의 사항이 있으시면 아래로 연락주시기 바랍니다.
Tel : 02-862-2816 / email : bio@usbio.co.kr